Импортерам стран ЕАЭС напомнили о новых правилах регистрации лекарств
Согласно установленным срокам, до 31 декабря 2025 года необходимо адаптировать ранее зарегистрированные препараты в соответствии с международными обязательствами и законодательными актами ЕАЭС.
Как указано в положении о ввозе лекарственных средств на территорию ЕАЭС, для помещения зарегистрированных препаратов под таможенные процедуры (включая выпуск для внутреннего потребления, переработку, реимпорт и отказ в пользу государства) требуется предоставить таможенному органу информацию о включении препарата в реестр зарегистрированных лекарственных средств ЕАЭС или в местный реестр страны-члена ЕАЭС.
Для осуществления выпуска препаратов наличие действующей записи в реестре является обязательным.
Читайте также:
Для Ала-Букинского ЦОВП построят склад лекарственных средств за 11,2 млн сомов
Ала-Букинский межрайонный Центр общеврачебной практики запустил тендер на возведение склада для...
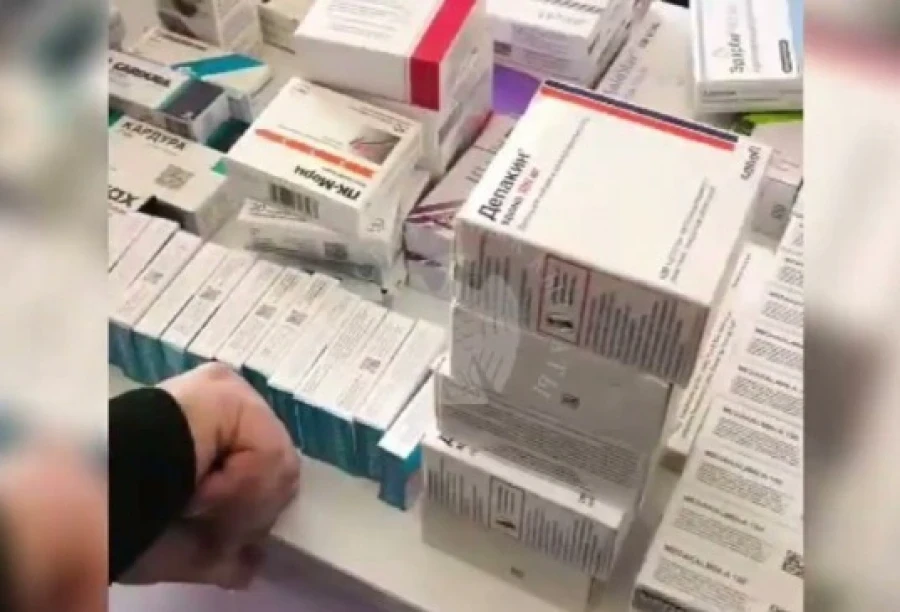
Налоговики выявили в Оше нелегальную партию лекарств
В аптеке были найдены препараты, реализуемые без лицензии В городе Ош сотрудники Государственной...

В Бишкеке раскрыт канал сбыта психотропных препаратов — задержана фармацевт
В Бишкеке был пресечен канал, занимающийся незаконной продажей психотропных и сильнодействующих...

Рейд в городе Ош. Налоговая служба выявила партию незаконных лекарств
В рамках рейдового контроля сотрудники Налоговой службы Кыргызской Республики в Оше обнаружили...

В Бишкеке задержали фармацевта аптеки за контрабанду и сбыт психотропных препаратов
В жилище женщины была обнаружена крупная партия контрабандных сильнодействующих препаратов В...
Регистрация авто стала приносить значительно больше денег в бюджет
С января по сентябрь 2025 года Кыргызстан получил от регистрации автомототранспортных средств 3...
Через приложение «Дары-Дармек» можно пожаловаться на завышенные цены на лекарства, - ДЛО
Заведующий отделом информационной и технической поддержки Департамента лекарственных средств и...
Приложение по поиску лекарств обновят. Что изменится для пользователей
Нурадин Канатаев, заведующий отделом информационной и технической поддержки Департамента...
В Кыргызстане сохраняется контрабандный ввоз лекарств, - ДЛО
пр, заявил Нурадин Канатаев, заведующий отделом информационной и технической поддержки Департамента...
Ввоз товаров из Кыргызстана без маркировки ЕАЭС временно разрешил Путин
Президент России Владимир Путин подписал указ, временно разрешающий ввоз товаров из Кыргызстана и...
В КР обсуждают изменения в порядок учета импортных товаров в рамках ЕАЭС
Кабинет министров Кыргызской Республики инициировал общественное обсуждение проекта, касающегося...
Китай с 1 января 2026 года вводит жесткие ограничения на экспорт новых автомашин
С 1 января 2026 года Китай вводит новые строгие правила для экспорта новых автомобилей, которые...
Ежегодно в Кыргызстан завозят лекарства на 30 миллиардов сомов
По информации Нурадина Канатаева, который возглавляет отдел информационной и технической поддержки...
В Казахстане с 1 июля 2026 года мигрантов будут регистрировать по новым правилам
В Казахстане вступят в силу новые правила регистрации мигрантов. Это стало известно благодаря...

При вступлении в ЕАЭС кыргызстанцы смогут ввозить автомобили по прежним таможенным ставкам до 2020 года
Однако желающие продать автомобиль в страны ЕАЭС должны будут доплатить до уровня ставок...
"Продают из-под прилавка". Некоторые аптеки продолжают снабжать "аптечных наркоманов"
На брифинге, посвященном вопросам борьбы с "аптечной наркоманией", начальник отдела...
Сертификаты соответствия, выданные в Кыргызстане, подвергают сомнению в России
Как сообщает «Коммерсант», Росаккредитация приняла решение об отзыве сомнительных сертификатов,...
В Бишкеке выявлена аптека, где занимались контрабандой и сбытом психотропных и сильнодействующих лекарств
Согласно информации, предоставленной пресс-службой СБНОН МВД, 28 октября в Бишкеке был пресечен...
Выплаты Кыргызстану по пошлинам от стран ЕАЭС продолжают снижаться
В период с января по сентябрь текущего года Кыргызстан получил от стран ЕАЭС 16 миллиардов 685,1...
Производство молока в Кыргызстане выросло на 2,7%, в целом по ЕАЭС – на 1,5% по итогам трёх кварталов
- В первом полугодии 2025 года объемы производства молока в Кыргызстане увеличились на 2,7% по...
Поправки в налоговое законодательство: Введены более высокие штрафы и конфискация за повторные нарушения при ввозе из ЕАЭС
- 29 октября 2025 года президент Садыр Жапаров подписал закон КР №243, который вносит изменения в...
В Кыргызстане изменили правила допуска иностранных автомобилей к эксплуатации
Кабинет министров Кыргызской Республики утвердил изменения в действующее постановление, касающееся...

Легкая промышленность под контролем: Минэкономики уточнило требования ЕАЭС
Важнейшим документом, регулирующим эти требования, является Технический регламент ТР ТС 017/2011...

Вступил в силу договор о Евразийском экономическом союзе
С 1 января 2015 года вступил в силу договор о Евразийском экономическом союзе (ЕАЭС). Договор о...
Доля Китая во внешнем товарообороте стран ЕАЭС достигает 35%, - ЕЭК
Директор Департамента торговой политики ЕЭК Владимир Серпиков поделился информацией о росте...
Армения и Кыргызстан демонстрируют наиболее высокий рост производства яиц в ЕАЭС по сравнению с прошлым годом
Евразийская экономическая комиссия (ЕЭК) опубликовала статистику по сельскому хозяйству...

В Кыргызстане вводят отдельный таможенный режим для товаров интернет-торговли
В Кыргызстане был принят закон, вносящий изменения в ряд норм, касающихся таможенного...
Каждый кыргызстанец может искать лекарства через мобильное приложение «Дары-Дармек», - ДЛО
Заведующий отделом информационной и технической поддержки Департамента лекарственных средств и...
Таможня РФ просит декларантов ЕАЭС ответственно выполнять обязательные процедуры
В последнее время в России наблюдается рост случаев использования документов, подтверждающих...
Кыргызстан сохранил лидерство в ЕАЭС по темпам роста строительства жилья
Согласно данным Евразийской экономической комиссии, в период с января по август объем строительных...
Кабмин разрешил «воздушный» экспорт лошадей, сохранив общий запрет на вывоз скота
. 15 октября 2025 года Кабинет министров подписал постановление № 668, которое обновляет условия...
В приложении «Дары-Дармек» можно пожаловаться на завышенные цены на лекарства
Мобильное приложение «Дары-Дармек» предоставляет возможность пользователям жаловаться на завышенные...

Китай вводит ограничения на экспорт автомобилей с 1 января 2026 года
С 1 января 2026 года Китай вводит новые правила, касающиеся экспорта автомобилей. Эти ограничения...
Принят закон о таможенном регулировании электронной торговли
- Законопроект №253 «О внесении изменений в некоторые законодательные акты по вопросам таможенного...

Зурдинов Аширалы Зурдинович
Зурдинов Аширалы Зурдинович (1946), доктор медицинских наук (1987), профессор (1990) Кыргыз....
В жилмассиве Бишкека открыли новый круглосуточный отдел регистрации авто
В Бишкеке открылся новый круглосуточный отдел регистрации автомобилей «Биримдик-24», который...
В Кыргызстане хотят продлить запрет на экспорт древесины
В Министерстве экономики опубликовали проект, который подразумевает продление запрета на вывоз...

Нацбанк Кыргызстана выпустил коллекционную монету ЕАЭС
Тираж коллекционной серебряной монеты, выпущенной Нацбанком КР, составил всего 1 тысячу штук......
В Москве обсудили формирование общего финансового рынка в рамках ЕАЭС
В Москве состоялась встреча, посвященная созданию общего финансового рынка в рамках Евразийского...
Госномера на авто немного изменились, их начали выпускать в Кыргызстане
В Кыргызстане стартовал выпуск новых государственных номеров для автомобилей, как сообщил 3 ноября...

Росаккредитация усиливает контроль за товарами из стран ЕАЭС
Согласно новым изменениям, внесенным в постановление Правительства РФ от 19 июня 2021 года № 936,...
Кыргызстан занял третье место в ЕАЭС по росту сельхозпроизводства
Согласно данным, опубликованным Евразийской экономической комиссией, в период с января по август...
В КР обсуждают ужесточение правил работы пунктов пропуска и учета товаров
На рассмотрение общественности представлен проект постановления кабинета министров, касающийся...